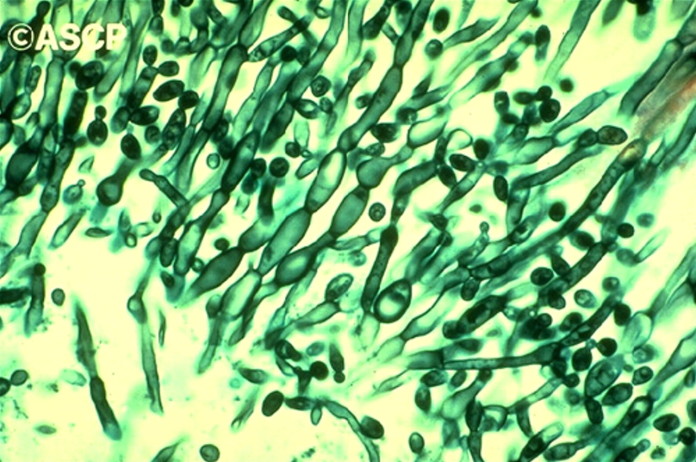

Los científicos están un paso más cerca de comprender cómo un hongo normalmente inocuo camba en un agente infeccioso mortal.
El hongo oportunista Candida albicans es normalmente un miembro de inofensiva de la comunidad microbiana que ocupa el intestino humano. Sin embargo, también es el agente causante de la candidiasis oral y, más gravemente, es responsable de aproximadamente 400.000 infecciones que amenazan la vida cada año. Entender lo que desencadena este cambio de residencia benigna de enemigo peligroso podría ayudar a proteger a las personas que están en mayor riesgo – incluyendo los pacientes de edad avanzada, el VIH y los que reciben trasplantes de órganos.
La mayor parte del tiempo, el sistema inmune humano es capaz de suprimir C. albicans de modo que vive en forma inocua, como una «levadura». Cuando el sistema inmunológico está comprometido, sin embargo – como por ejemplo durante los trasplantes de órganos para prevenir el rechazo de tejidos – los interruptores de hongos cambian a un nuevo y mortal modo de crecimiento. Las células redondas empiezan a producir filamentos largos (llamados hifas) que se introducen en las capas de tejido subyacentes. Esto permite al hongo invadir y formar colonias infecciosas.
Investigadores de la Universidad de Aberdeen han descubierto recientemente que una molécula de señalización pequeña, llamada RSR1, controla los mecanismos de dirección como las hifas sondean superficies de acogida. «RSR1 ayuda a las hifas penetrar en los tejidos y dirigirse a través de barreras», dice Tina Bedekovic, que estudia esta proteína como parte de su investigación. «Sin RSR1, la capacidad del hongo para causar la enfermedad se reduce significativamente». La levadura de cerveza (Saccharomyces cerevisiae) no forma filamentos pero todavía tiene funciones de RSR1 para controlar el crecimiento polarizado. En este caso, se sabe que puede ser activado por otra molécula llamada BUD5. Cuando los investigadores eliminan BUD5 en C. albicans, sin embargo, sus hifas eran todavía capaces de penetrar en los tejidos y conducir alrededor de obstáculos. Esto sugiere que RSR1 en C. albicans está regulado por un activador diferente específica para esta función.
Según Tina Bedekovic, identificando este activador puede ayudar a desarrollar tratamientos clínicos. «Los seres humanos también tienen una versión de RSR1 y BUD5 por lo que es poco probable que podamos desarrollar un fármaco para inhibir la C. albicans sin afectar también células humanas», dice. «Pero si son parte de una vía de señalización-hongo específico que controla el crecimiento direccional, esto podría ser dirigido con fármacos terapéuticos sin dañar al paciente».
Los investigadores ahora planean investigar el cual las moléculas se pueden unir a RSR1 en C. albicans y, de estos, para identificar el activador requerido para el crecimiento filamentoso invasiva.
microcefalia cirugia, animales que se regeneran, candida albicans, partos normales x la vajina, ev bajos, imagen de paciente en coma